近日,湖南师范大学生命科学学院动物多肽药物创制国家地方联合工程实验室丁小凤教授团队在中科院1区刊物《Cell Death & Disease》(IF: 9.6)发表最新研究成果“Deletion of Tfap2a in hepatocytes and macrophages promotes the progression of hepatocellular carcinoma by regulating SREBP1/FASN/ACC pathway and anti-inflammatory effect of IL10”,首次系统揭示转录因子AP-2α在肝细胞和巨噬细胞中调控脂质从头合成及炎症反应,在原发性肝细胞癌(HCC)中的关键作用与机制。

HCC是一种常见且致命的原发性肝脏恶性肿瘤,具有高度异质性和侵袭性,全球范围内病死率居高不下。尽管近年来治疗手段不断进步,但由于早期诊断困难、肿瘤进展迅速及耐药机制复杂,HCC患者的总体生存率仍然偏低。因此,深入挖掘其发生发展的关键分子机制,特别是涉及代谢重编程、免疫逃逸及炎症反应调控的环节,对于揭示HCC进展本质并探索新的治疗靶点具有重要意义。研究团队首先发现在DEN/CCl4诱导的HCC小鼠模型中AP-2α的mRNA和蛋白质水平下调。接着,构建了多种细胞类型特异性敲除Tfap2a的小鼠模型,包括肝细胞 (Tfap2aΔHep)、肝星状细胞 (Tfap2aΔHSC)和巨噬细胞 (Tfap2aΔMΦ)。Tfap2a 的敲除会促进 Tfap2aΔHep 和 Tfap2aΔMΦ 小鼠发生不同程度的肝脂肪变性,但对 Tfap2aΔHSC小鼠肝脏无明显影响。在DEN/CCl4诱导的HCC小鼠模型中,Tfap2aΔHep 和Tfap2aΔMΦ 小鼠表现出更严重的肝脂肪变性及更多的肝脏肿瘤结节。
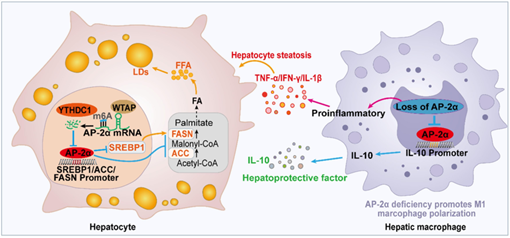
机制研究表明,AP-2α可直接结合脂质从头合成关键酶SREBP1、ACC和FASN的启动子,抑制其表达,进而减少肝细胞内脂滴积累。同时,在巨噬细胞中,Tfap2a缺失促进其M1型极化,降低抗炎因子IL-10表达,增强促炎反应,加剧肿瘤微环境恶化。此外,研究还发现m6A甲基化修饰通过WTAP/YTHDC1介导,降低AP-2α mRNA稳定性,是其在HCC中表达下调的分子机制之一。临床样本分析进一步表明,随着NAFLD、NASH到HCC的进展,AP-2α表达逐渐下调,而WTAP、YTHDC1和FASN表达上调,提示m6A修饰可能介导了AP-2α的下调并参与炎症向肝癌的演变过程。
该研究表明,AP-2α不仅在脂质代谢和炎症反应调控中起核心作用,也是HCC潜在的多功能治疗靶点,为脂代谢紊乱及慢性炎症驱动的肝癌治疗提供了新的理论依据与干预策略。
该研究论文以湖南师范大学为第一署名单位,丁小凤教授为唯一通讯作者, 2023年毕业的博士生李志伟(现为北京大学国际癌症研究院博士后)为第一作者。研究获得国家自然科学基金、国家重点研发计划、湖南师范大学交叉科学研究院培育团队项目、湖南省企业科技特派员计划项目、湖南省区域遗传性出生缺陷重点实验室开放研究基金以及湖南省重点研发专项等多项资助。
论文链接:https://www.nature.com/articles/s41419-025-07500-8
